Bộ Y tế đề nghị kiểm định mẫu vắc-xin gây tai biến
Trước thông tin 3 trẻ em ở Nghệ An tử vong sau khi tiêm vắc-xin 5 trong 1, Cục Y tế dự phòng (Bộ Y tế) đã có văn bản gửi Tổ chức Y tế Thế giới đề nghị kiểm định mẫu lưu vắc-xin “5 trong 1” Quinvaxem của Hàn Quốc.
Thông tin được Cục Y tế dự phòng (Bộ Y tế) cho biết ngày 24/12.
Việc kiểm định này sẽ được thực hiện đối với mẫu lưu vắc-xin ở Việt Nam. Cục Y tế dự phòng cũng đề nghị nhà sản xuất vắc-xin ở Hàn Quốc cung cấp thông tin vắc-xin này đã được sử dụng ở những quốc gia nào, các phản ứng liên quan...
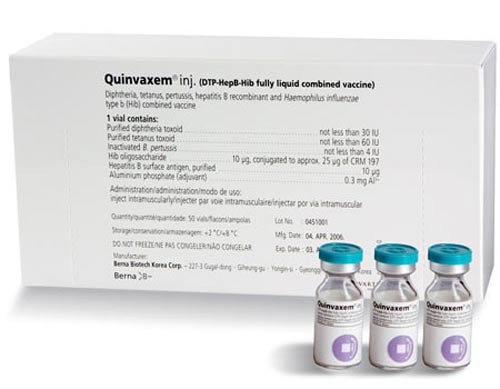
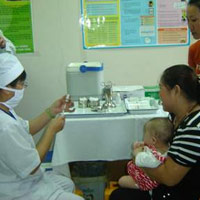
Vắc-xin Quinvaxem gây tai biến cho 3 trẻ tại Nghệ An
Cùng ngày, Cục Quản lý Dược cũng có công văn yêu cầu nhà sản xuất (Công ty Berna Biotech Korea Corporation - Hàn Quốc), nhà nhập khẩu cùng nhà phân phối loại vắc-xin này phải báo cáo về tình hình nhập khẩu và quá trình phân phối vắc-xin trên về Cục Quản lý Dược trước ngày 25/12.
Vắc-xin Quinvaxem (ngừa 5 bệnh bạch hầu, ho gà, uốn ván, viêm gan siêu vi B và Hib) do Hàn Quốc sản xuất được đưa vào chương trình tiêm chủng mở rộng từ tháng 6-2010, tiêm cho trẻ 2, 3 và 4 tháng tuổi. Các thống kê cho thấy đến thời điểm này đã có gần 30 trường hợp có phản ứng nặng sau tiêm vắc-xin Quinvaxem.
Ngoài ra, Cục Quản lý Dược đưa ra thông báo tạm ngừng việc sử dụng lô vắc-xin trên và yêu cầu Sở Y tế các tỉnh, thành phố trực thuộc Trung ương, Y tế các ngành, các Trung tâm y tế dự phòng tỉnh, thành phố trực thuộc Trung ương thông báo cho các cơ sở kinh doanh, sử dụng vắc xin tạm ngừng sử dụng lô vắc xin đã nêu.
Vắc-xin Quinvaxem do Hàn Quốc sản xuất, được Liên minh toàn cầu về vắc-xin và tiêm chủng (GAVI) tài trợ cho Việt Nam thông qua Quỹ Nhi đồng Liên Hiệp Quốc từ năm 2010. Từ năm 2010 đến nay, Việt Nam đã sử dụng trên 13 triệu liều Quinvaxem.